Сульфур і Хлор – елементи третього періоду, протонне число Хлору більше за протонне число Сульфуру, тож електронегативність Хлору також більша.
Флуор — найбільш електронегативний елемент, за ним іде Оксиген (3,5) і далі Нітроген і Хлор (3,0).
Зі збільшенням порядкового номера елементів ЕН змінюється періодично. У періоді вона зростає зліва направо при накопиченні електронів на зовнішньому шарі. У групі вона знижується згори донизу при збільшенні числа електронних шарів і збільшенні атомних радіусів.
Електронегативність фтору Фтор є найбільш електронегативним елементом, оскільки він має 5 електронів у своїй 2P оболонці. Оптимальна електронна конфігурація орбіти 2P містить 6 електронів, тому оскільки фтор настільки близький до ідеальної електронної конфігурації, електрони тримаються дуже щільно до ядра.
Йод
| Йод (53I) | |
|---|---|
| Класифікація | галоген |
| Властивості атома | |
| Атомний номер | 53 |
| Атомна маса (молярна маса) | 126,90447 а.о.м. (г/моль) |
Періодичність властивостей елементів Атомний радіус — збільшується зверху до низу і зменшується зліва направо (в елементах головних груп) Електронегативність — зменшується зверху до низу і збільшується зліва направо (виняток Інертні гази) Енергія іонізації — зменшується зверху до низу і збільшується зліва направо
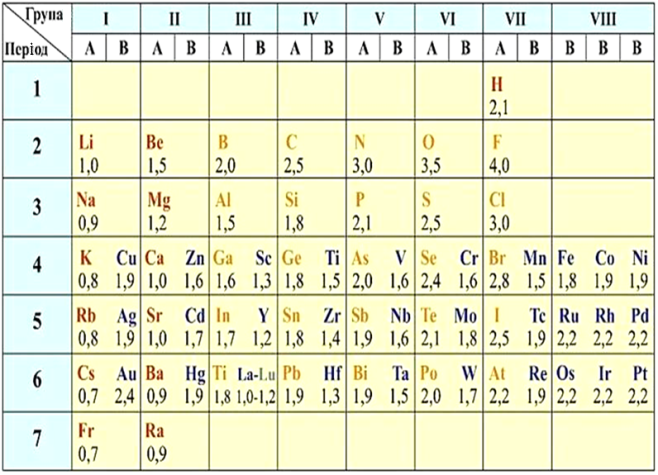

Електронегативність показує здатність елементів віддавати або приймати електрони. Ця характеристика допомагає зрозуміти, …